Bioteknologiaren sektoreak Europan 5.489 milioi euro mugitu zituen 2020ko lehen hiruhilekoan, eta 4.811 milioi bigarrenean. Guztira, 10.300 milioi euro, 2019an baino % 9,5 gehiago. Egia esan, oso sektore emankorra da, ezinbestekoa izateaz gain, baina ez da sektore erraza Europan.
Etengabe ari gara EBn aldaketak izaten, merkaturatzeko zailtasunak areagotzen dituztenak: brexit-ak Erresuma Batuak legeria propioa izatea eragin du, eta Suitzak, bere aldetik, ez du berritu produktu bat bere lurraldean EBn bezala merkaturatzea ahalbidetzen zuen lankidetza-akordioa. Horregatik, herrialde horietan merkaturatzeko arau berriak bete behar dira orain.
Hala ere, fabrikatzailearen trebetasunarekin eta ezagutzarekin, edo deviCE Sistemas bezalako aholkularitza-enpresa espezializatu on baten laguntarekin, lege-zailtasun horiek gainditu daitezke. Fabrikatzaile batentzat benetako zailtasunak, orain, Europako araudi berrietan eta horiek betetzen diren ebaluatzeko erakunderik ezean daude.
Sektore bioteknologikoak Espainian duen egoera antzekoa da: AseBioren 2019eko txostenaren arabera, sektore bioteknologikoak ia 12.000 milioi euroko fakturazioa eragin du, BPGren % 1. Enpresa horien % 51 Espainian mikroenpresak dira, 10 langile baino gutxiago dituzte, eta % 45 enpresa txiki eta ertainak dira, batez ere Katalunian, Madrilen, Andaluzian eta Euskal Autonomia Erkidegoan. Biotech-ak nagusi dira produkzioaren hazkunde-rankingean, % 20,8ko hazkundearekin eta produktibitatearekin.

Lege berriak eta erakunde jakinaraziak
In vitro diagnostikorako osasun-produktuei eta osasun-produktuei buruzko Europako legedi berria indarrean sartzearekin batera, nabarmen gogortu dira erakunde jakinarazien egiaztapenerako betekizunak. Jakinarazitako erakundea (aurrerantzean ON) organismo independentea da, eta produktu batek eta enpresa batek aplikatzen dizkioten legezko baldintzak betetzen dituzten ebaluatzen du.
2021eko maiatzaren 26an, osasun-produktuak Europar Batasunean merkaturatzeari buruzko legea aplikatu zen, orokorrean osasun-produktuen CE marka bezala ezagutzen dena. Lege honen bidez, osasun-produktuak fabrikatzen dituzten enpresa guztiak ON batek ebaluatu behar ditu, baldin eta, beren ezaugarriak direla-eta, nolabaiteko arriskua badute.
Egoera hori, printzipioz, ez da indargabetutako legeekin gertatzen zenaren desberdina, horiekin ere beharrezkoa baitzen kasu horietan ON batek ebaluatzea. Hala ere, ON bat akreditatzeko baldintzak gogortzearen ondorioz, legeria berriaren araberako produktuak ebaluatzeko onartutako egungo kopurua oso urria da dagoen eskariarentzat.
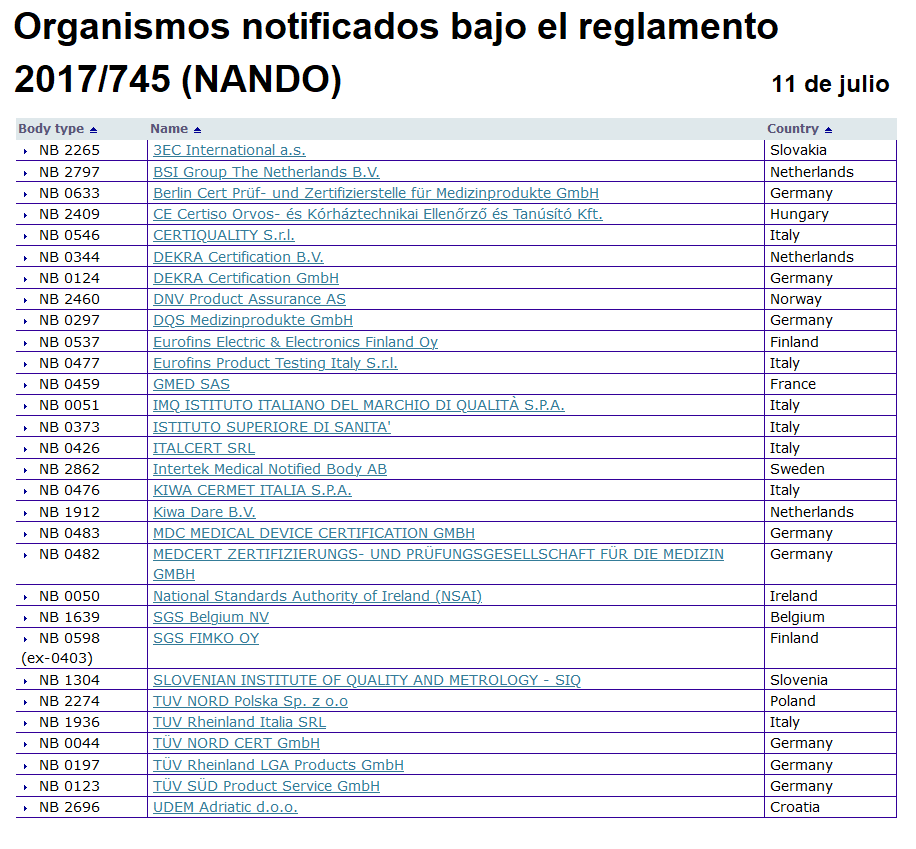

ON horiek, gaur egun, hiru ebaluazio-egoeratan dauden produktuei eman behar diete arreta: alde batetik, merkaturatzeko aurreko legeen arabera ONen oniritzia zuten produktu guztiek (CE adostasun-ziurtagiria) ziurtagiri iraungia edo iraungitzear dute gaur egun, eta horrek esan nahi du produktu horiek guztiak berriro ebaluatu behar direla.
Beste alde batetik, aurreko araudiarekin arrisku txikiko produktu gisa sailkatzen ziren osasun-produktu askok (hau da, fabrikatzaileak autozertifikatuak izan zitezkeenak) orain araudi berri bati egin behar diote aurre, eta araudi horrek orain ON batek ebaluatu behar dituen produktuen artean sartzen ditu, garapen berriko osasun-produktu guztiei gehituta; produktu horien ezaugarriak direla-eta, ON batek ebaluatu beharreko produktutzat hartzen dira.
Kontuan hartuta arau-aldaketa bat izan dela, eta ON bezalako erakundeak akreditatzeko eskakizunak gero eta zorrotzagoak direla, eta horrek erakunde ziurtatzaile horien urritasuna ekarri duela, gero eta zailagoa da produktu mota horien CE ziurtapenerako errealitatea, merkaturatzeko ezinbestekoa baita.
Produktu berritzaile bat duen eta zailtasun handiko produktu gisa sailkatuta dagoen enpresa fabrikatzaile batek, beharbada, ON bat edo bi baino ez ditu akreditatuta produktu hori ebaluatzeko, eta horrek zaildu egiten du ziurtapena eta merkaturatzea.
2022ko maiatzaren 26an, in vitro diagnostikorako osasun-produktuei buruzko Europako legea aplikatu zen. Horrek esan nahi du osasun-produktuetarako gertatzen ari den guztia in vitro diagnostikorako gailuekin gertatuko dela, baina areagotu egingo dela. Osasun-produktuak ON gutxi baditu, harrigarria bada ere, gaur egun 7 ON akreditatu baino ez ditugu in vitro fabrikatzaile guztiei zerbitzua emateko.
Azken batean, bioteknologien sektorea gorantz doan sektorea da, eragin ekonomiko handikoa, I+Gn eta ezagutza espezializatuan. Hala eta guztiz ere, arau-aldaketen ondorioz enpresa horiek izaten ari diren zailtasunak nabarmenak dira eta dezelerazioa eragin dezakete.
Euskadi da sektore hori gehien garatzen ari den Espainiako eskualdeetako bat, bai I+Gko inbertsioan, bai ezagutza espezializatuan. Enpresa askok ahalegin handia egin dute osasun-produktuen eta in vitro produktuen garapenean, baina ahalegin hori ez da sarituko erregulazio-prozesuak errazten ez badira.
On izan nahi duten erakundeen ebaluazio-prozesuak sinplifikatzeko premia larria dago. Egia esan, Europako Batzordeak ahalegin handia egin du in vitro produktuen legezko baldintzak betetzeko luzamenduak ahalbidetuz, baina ez da nahikoa. Euskadiko lankidetza publiko-pribatuak fruituak eman ditu iraganean, eta oso tresna interesgarria izan daiteke prozesu zorrotz, zehatz, arin eta azkar batean ON izan nahi duten erakunde espezializatuak garatzeko.








